| предыдущая |
вверх
|
следующая
|
Видимо, самым популярным предположением о состоянии газа или газообразного вещества, является модель идеального газа. (иногда добавляют одноатомного газа, но в нашем рассмотрении это несущественно). Дать последовательное определение, какой газ и при каких условиях можно считать идеальным, может оказаться довольно сложным. Поэтому иногда имеет смысл поступить наоборот - определить сам идеальный газ как такой газ, который подчиняется уравнению состояния идеального газа!
В действительности, многие вещества в газообразном состоянии проявляют свойства, близкие к предсказываемым для идеальных газов. Таковы все нормальные газы при комнатных температурах и плотностях, вдали от точек конденсации. Однако нас интересует вычисление давления в условиях, весьма далеких от комнатных - в недрах звезд при температурах миллионов и миллиардов градусов, и плотностях, в десятки и сотни тысяч раз превышающих плотности воздуха в земных условиях. Несмотря на столь существенную разницу, идеальный газ черезвычайно популярен при теоретических описаниях звездного вещества. Это как бы отправная точка, нулевое приближение, на фоне которого мы начинаем свои расчеты.
Уравнение идеального газа в отношении его давления записывается обычно в виде
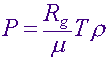
В этом выражении Rg - универсальная газовая постоянная, а T - температура и r -плотность. Особую роль играет m -молекулярный вес вещества. В обычном состоянии газы состоят из атомов и молекул, и молекулярный вес связан с весом каждой частицы. Если вещество звезды предполагается в нейтральном состоянии, то молекулярный вес можно вычислить через используемые в астрофизике относительные удельные (весовые) содержания водорода X, гелия Y и элементов тяжелее гелия Z в виде
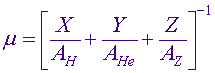
Однако в нормальном состоянии вещество в звездах встречается довольно редко, поэтому такое выражение имеет не большого значения. Более распространенным случаем является ситуация полной ионизации атомов, что снова означает идеальный газ, но с другим молекулярным весом,
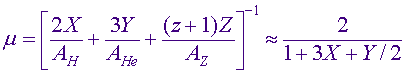
(В выражениях для молекулярного веса Ai атомный вес соответствующей компоненты, а z - средний заряд для компонент тяжелее гелия).
В перечисленных случаях мы имеем дело с "эмпирическим" подбором уравнения состояния для исследуемого объекта - просто считается (или проверяется экспериментально), что давление газа близко к тому, что получается из уравнения идеального газа. В астрофизических приложениях уравнение идельного газа играет значительно большую роль, если его использовать при вычислениях давления отдельных компонент, составляющих рассматриваемый газ. Очевидно, что вещество звезд состоит из различных атомов и ионов, и можно рассматривать парциальные давления, создаваемые каждой из компонент. Более того, по закону Дальтона, мы можем ожидать, что общее давление оказывается равным сумме парциальных - этот закон строго справедлив для идеальных газов. Но в этом случае область применимости идеального уравнения хотябы для отдельных компонент значительно расширяется. В очень большом диапазоне температур и плотностей давление, создаваемое атомами и ядрами ионов (атомными остатками) описывается формулой для идеального газа, которую, правда, переписывают в виде
В этом выражении ni - концентрация частиц i-го сорта (штук в см3), а k - это постоянная Больцмана. Легко видеть, что ni - концентрации атомов и ионных остатков легко вычислить, зная плотность и относительное содержание данного атома - водорода, гелия и др. Если известно, что вещество нейтрально, то концентрация свободных электронов ne просто равна нулю (и, соответственно, равно нулю компонент электронного давления), а если вещество полностью ионизованно, то эту концентрацию также можно вычислить по концентрациям ядер всех сортов
Общее давление полагается равным просто сумме отдельных компонент - это приближение имеет достаточно глубокие корни в статистической физике. Таким образом
(роль и смысл других компонент давления мы обсудим в следующих параграфах). Но в рамках обсуждаемых предположений, такое выражение остается эквивалентным уравнению состояния идеального газа.
Механическая модель для идеального газа
Статистическая модель идеального газа
| предыдущая |
в
начало
|
следующая
|